

 |
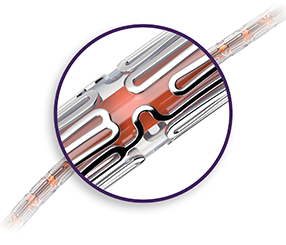
sistema de stent farmacológico xience sierra™O mais novo DES (Stent Farmacológico) na família XIENCE™, XIENCE Sierra™ apresenta um design aprimorado que oferece capacidades excepcionais de liberação, amplificação e expansão pós-dilatação, bem como perfil ultrabaixo e passagem mais suave.4 |
RESUMO DAS CARACTERÍSTICAS
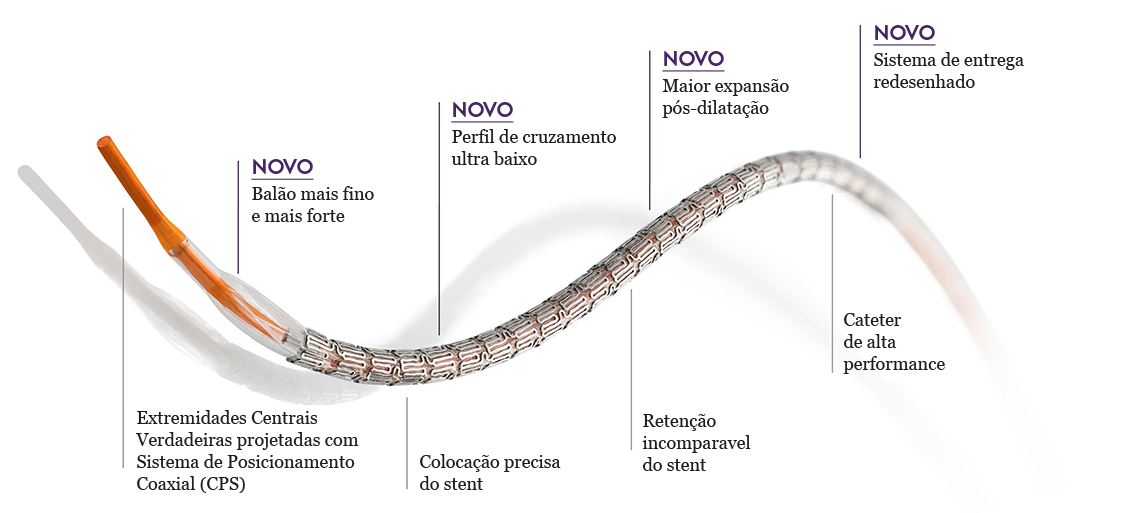
As características do XIENCE Sierra™ incluem os elementos de design aprimorados mais modernos.5
XIENCE, PADRÃO DE EXCELÊNCIA PARA A SEGURANÇA
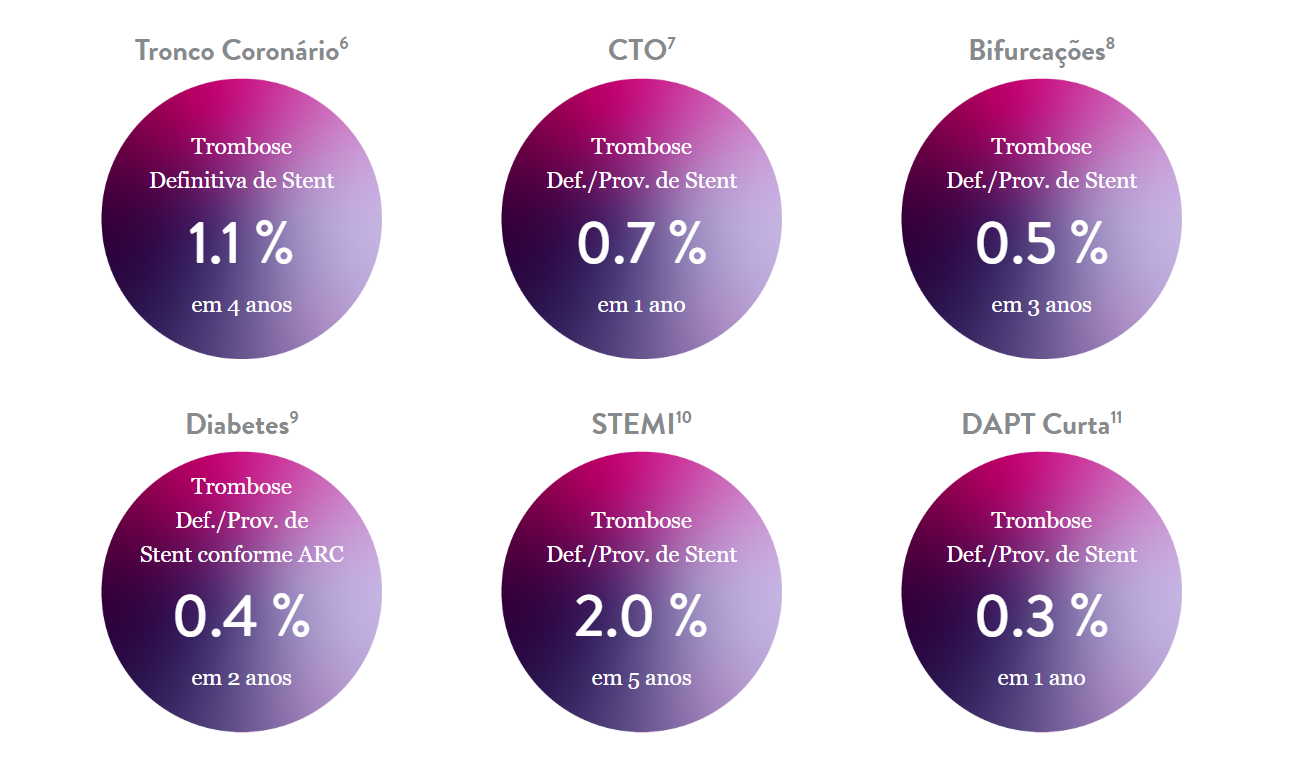
Taxas consistentemente baixas de trombose do stent
Como o líder mundial em stents farmacológicos5, o XIENCE Sierra™ é padrão de excelência para segurança na implantação de stents. Estudos clínicos randomizados e multicêntricos revelam a eficácia e segurança do uso de XIENCE™ mesmo em intervenções coronarianas percutâneas (ICP) complexas. Os dados de segurança são particularmente irrefutáveis graças às taxas de trombose do stent (TS), com dados de estudo clínico de longo prazo de até 5 anos.6-11
Segurança para Cruzar Anatomias Desafiadoras
Mesmo ao se deparar com uma anatomia difícil em determinados casos, há melhor retenção de stent com o XIENCE Sierra™ em comparação aos demais stents, como demonstrado.5
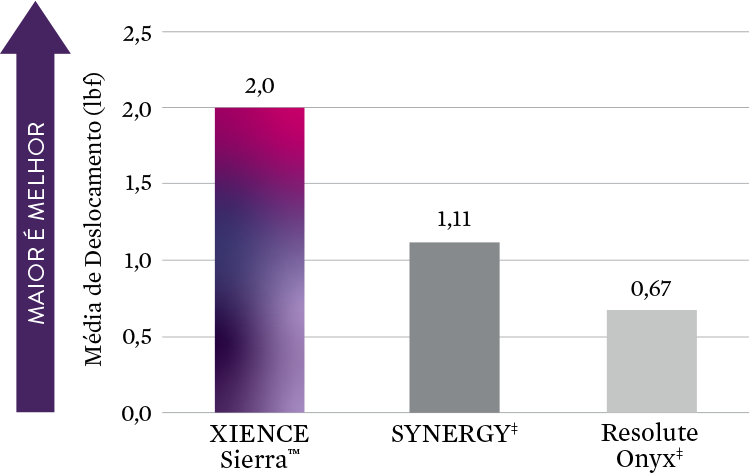
 |
XIENCE pro™a SISTEMA DE STENT CORONARIANO ELUÍDO EM EVEROLIMUSXIENCE Pro™ A, como todos os stents XIENCE™, apresenta uma combinação exclusiva de design, medicamento e fluoropolímero — com o revestimento de fluoropolímero mostrando-se ser significativamente mais antitrombótico que os demais stents farmacológicos.12 |
OS FUNDAMENTOS BASE DE XIENCE Pro™ a
XIENCE Pro™ A é indicado para ser utilizado por cardiologistas intervencionistas para tratar lesões complexas do dia a dia.
Precisão na inserção do Stent
O design MULTI-LINK, com 100% de inserção exata de stent entre marcadores intermediários, oferece implantação precisa
Verdadeira Extremidade Central
Design de extremidade flexível com sistema de posicionamento coaxial (CPS) oferece desempenho máximo em lesões complexas
Cateter de Desempenho mais Elevado
O cateter é projetado para otimizar a resistência, flexibilidade e capacidade de expansão
- Eixo distal de transição zero
- Hipotubo robusto com espessura otimizada
- Membro externo especialmente formulado
Balão durável com conformidade plana
Balão fino e dupla camada possibilita implantação de alta pressão enquanto mantém a flexibilidade de resistência.
DESIGN EXCLUSIVO POR TRÁS DOS DADOS DE SEGURANÇA DE XIENCE™
Todos os componentes do XIENCE Pro™ A são projetados para segurança.

- Zanchin C, et al. JACC Cardiovasc Interv. 2019;12(17):1665-1675. • Serruys P, et al. N Engl J Med. 2010;363(2):136-146. • Shiomi H, et al. JACC Cardiovasc Interv. 2019;12:637-647. • Kufner S, et al. Circulation. 2019:139(3):325-333. • Palmerini T, et al. Lancet. 2012;379(9824);1393-1402. • Bangalore S, et al. Circ Cardiovasc Interv. 2013;6:378-390. • Pilgrim T, et al. Lancet. 2014;384:2111-2122. • Pilgrim T, et al. Lancet 2018;392:737-746.
- Dados em arquivo na Abbott. Os 15 milhões de implantes baseiam-se nos dados de DES até o primeiro trimestre de 2020.
- Kufner S, et al. Circulation. 2019:139(3):325-333. Shiomi H, et al. J Am Coll Cardiol Interv. 2019;12:637-647.
- Testes realizados por e dados em arquivo na Abbott
- Testes realizados por e dados em arquivo na Abbott:
- Declaração de design aprimorado é comparada ao Stent XIENCE Pro™ A
- Capacidade de passagem do desempenho do cateter se refere ao teste realizado no Stent XIENCE Sierra™ (3,0 x 18 mm) n = 5, Stent SYNERGY‡ (3,0 x 20 mm) n = 5, Stent Resolute Onyx‡ (3,0 x 18 mm) n = 5. Teste de capacidade de passagem de desempenho de cateter mede a força média para cruzar um modelo de lesão desafiadora. Os dados do teste de bancada demonstram que XIENCE Sierra™ se desempenhou melhor quanto à capacidade de passagem e não foi estatisticamente diferente nas capacidades de rastreabilidade e expansão em comparação aos stents Resolute Onyx‡ e SYNERGY‡. Resultados do teste de bancada podem não necessariamente ser indicados de desempenho clínico.
- Aumento da expansão máxima em comparação aos demais sistemas de Stent coronariano eluídos em Everolimus XIENCE™.
- Ampliação de opções de tratamento com a expansão pós-dilatação de até 5,5 mm (3,5-4,0 mm) e matriz de tamanho mais completa para lesões cônicas longas. Acessibilidade de ramo lateral com diâmetro robusto (3,0 x 18 mm) para tratar bifurcações. Resistência radial potencializada em tamanhos robustos para lesões altamente calcificadas (em comparação às gerações anteriores).
- Perfil frisado ultrabaixo de 0,0390" se refere ao tamanho de perfil do Stent XIENCE Sierra™ de (3,0 x 18 mm) n = 5, Stent SYNERGY‡ (3,0 x 20 mm) n = 5, Stent Resolute Onyx‡ (3,0 x 18 mm) n = 5.
- Declaração de encurtamento se refere ao teste realizado em um stent de 4,0 mm de diâmetro implantado em 5,5 mm. stent XIENCE Sierra™ (4,0 x 18 mm) n=5, Stent Synergy‡ (4,0 x 20 mm) n=5, Stent Resolute Onyx‡ - (4,5 x 18 mm) n=5, Stent Orsiro‡ (4,0 x 18 mm) n=5.
- Aumento de expansão máxima em comparação ao outro Sistema de stent coronariano eluído em Everolimus XIENCE™.
- Teste de retenção é medido pela média de deslocamento (lbf).
- Stone, G. EXCEL: estudo clínico prospectivo e randomizado que compara os stents eluídos em everolimus e cirurgia de revascularização em pacientes selecionados com doença da artéria coronária principal esquerda. TCT 2018.
- Teeuwen, K. et al. Estudo clínico randomizado e multicêntrico que investiga resultados angiográficos de stents híbridos eluídos em sirolimus com polímero biodegradável em comparação aos stents eluídos em everolimus com polímero durável em oclusões totais crônicas (PRISON IV). JACC Cardiovasc Interv. 2017;10(2):133-143. doi:10.1016/j.jcin.2016.10.017.
- Lam, M. Resultado de estudo clínico de três anos de duração de pacientes com tratamento de bifurcação com stents de segunda geração Resolute e XIENCE V no estudo clínico randomizado TWENTE. Am Heart J. 2015;169.
- Kaul U, et al. Stents eluídos em paclitaxel versus stents coronarianos eluídos em everolimus em uma população diabética: acompanhamento de dois anos de duração do estudo clínico TUXEDO-Índia. EuroIntervention. 2017:13:1194-1201.
- Sabaté M, et al. Estudo clínico EXAMINATION. Lancet. 2016;387;357-366.
- Watanable, H. et al. Efeito da terapia antiplaquetária dupla de 1 mês de duração seguido de clopidogrel vs terapia antiplaquetária dupla de 12 meses de duração em eventos cardiovasculares e de sangramento em pacientes recebendo ICP: Estudo clínico STOPDAPT2. JAMA. 2019;321(24):2414-2427. doi:10.1001/jama.2019.8145.
- Jinnouchi H, et al. J Am Coll Cardiol. 2019;74:Suppl B – TCT-291.
- Colombo A, et al. JACC. 2002;40:1021-1033.
- Dados em arquivo na Abbott.
- Kolandaivelu K, et al. Circulation. 2011;123;1400-1409.
- Kastrati A, et al. Circulation. 2001;103;2816-2821.
- Perkins LEL, et al. J Interv Cardiol. 2009;22(s1):S28-S40.
- Otsuka F, et al. JACC Cardiovasc Interv. 2015;8:1248-1260. doi: 10.1016/j.jcin.2015.03.029.
- Otsuka F, et al. Circ Cardiovasc Interv. 2014;7:330-342.
- Ding N, et al. J Interv Cardiol. 2009;22(s1):S18-S27.
- Joner M, et al. J Am Coll Cardiol. 2008;52(5):333-432. doi: 10.1016/j.jacc.2008.04.030.
- Guidoin R, et al. ASAIO J. 1994;40(3):M870-M879.
- Paton et al.; U.S. Patent 5,356,668.
- Lilenfeld et al.; U.S. Patent 4,564,013.
- Tu et al.; U.S. Patent 4,816,339.
- Lo et al.; U.S. Patent 3,178,399.
- Panchalingam V, et al. ASAIO J 1993;39:M305-M309.










*Disponible en tamaño de balón de 3,5 a 5,0 mm
Datos archivados en Abbott.

MAT-XXXXXXX

